分子シャペロン
【分子シャペロンとは】 分子シャペロンはタンパク質のフォールディングを助ける利他的なタンパク質として定義されました。今では、フォールディングに留まらず、細胞内での「タンパク質の一生」を支える存在感のある脇役として知られています。
以下はもう少し詳しい解説です。
【アンフィンゼンのドグマ】 1950年代ごろ、Anfinsenらは、できあがった酵素(例えば、Ribonuclease A)に尿素(タンパク質変性剤として使用)を加えて酵素活性を失わせたあとに、尿素を透析で除去すると、元と同じ活性が回復することを見出しました。これにより、「タンパク質の立体構造はアミノ酸配列さえ決まれば決定する」、別の言い方をすると、「タンパク質はエネルギー最小の状態に勝手に折れたたむ(フォールディングする)」というアンフィンゼンのドグマが確立しました。アミノ酸の配列はDNAにコードされているわけですから、DNA→RNA→タンパク質の生命のセントラルドグマの最終過程であるmRNAの情報がリボソームでタンパク質の合成に翻訳されたあと、タンパク質は「勝手に」形ができる、すなわちフォールディングすることになります。フォールディングを実際に目で見てみるために行ったのが、緑に光るGFPタンパク質のフォールディング実験です。写真に示すようにGFP溶液のpHを塩酸で下げると瞬時に変性して緑色が消えます(真ん中が少し濁っているのは変性後に凝集ができてしまったからです)。そのあとに緩衝液を加えて中性に戻すと緑色が徐々に戻ります。(動画もあります → 目で見るGFPフォールディング実験)
このようにAnfinsenの実験は試験管内で行われましたが、細胞内でもタンパク質は勝手にフォールディングする、と長らく信じられてきました。
しかし、事はそれほど単純ではありません。
【フォールディング vs.凝集体形成】 まずは実験を見てください。上記のように変性したGFPはほぼ元通りにフォールディングします(→GFPフォールディング動画)。しかし、RFP(赤色蛍光タンパク質)では同じ実験をしても全然赤色蛍光が戻りません(→RFPフォールディング動画)。代わりに白く濁ってしまいます。つまり、タンパク質の凝集体ができます。
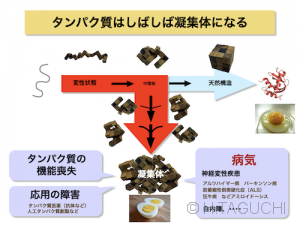
通常の球状タンパク質の場合、内部は疎水的なアミノ酸がコアを形成していますが、フォールディングの途上では疎水的な領域が露出します。疎水的なもの同士は集まろうとする性質(疎水相互作用)がありますので、「分子内」で疎水相互作用がはたらけば本来のフォールディングに導かれますが、「分子間」だと凝集体を形成してしまいます(フォールディング vs.凝集形成)。
通常、タンパク質の凝集体形成は不可逆なので、凝集になってしまうとせっかく合成されたポリペプチドも役立たずとなってしまいます。凝集体形成は高次の「分子間」反応なので、濃度が薄い状態でフォールディングさせれば凝集は起こりません。しかし、タンパク質が活躍する細胞内は、タンパク質をはじめとする生体高分子でたいへん混み合っていることが知られています(細胞内でタンパク質などがひしめくようすのイラスト)。
【分子シャペロン】 さまざまな物質で混み合った細胞内で、フォールディング途上の不安定な中間体や熱で変性したタンパク質が凝集にならないようフォールディングを助けているタンパク質が存在します。これが分子シャペロン(molecular chaperone)です。
シャペロンの概念は、シャペロニン(GroEL、Hsp60、CCTなど)やHsp70/DnaKなど今で言う主要シャペロンの細胞内でのはたらきがわかってきた1980年代後半に提唱されたものです。提唱者のJohn Ellisによる分子シャペロンの元々の定義は、「他のタンパク質の構造形成を助けるが、自らはその最終成分にならないタンパク質」となります。
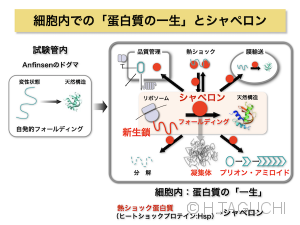
【「タンパク質の一生」、「タンパク質の社会」】 シャペロンの概念は、タンパク質のフォールディングを助ける機能から産まれてきたものですが、その後、細胞内でタンパク質が関わるさまざまな事象にシャペロンが関わることが次々と明らかになってきました。タンパク質がリボソームで合成されてくるところを「誕生」とすると、フォールディングして「一人前に成長」、ちがう場所に「移動」、緊急事態による「ストレス」、「老化」によるアミロイド形成、最期には「死」に至る、・・・。このように、タンパク質が合成されてきてから分解に至るまでを「一生」に例えると、「タンパク質の一生」のさまざまな局面でシャペロン的なタンパク質が陰に日向に手助けをしていることがわかってきました。つまりは、タンパク質は一人で勝手に産まれて勝手に死ぬのでなく、タンパク質同士の濃厚な「社会」の中で「一生」を過ごしていく、という概念にまで発展してきました。
タンパク質を理解する上で、シャペロンを理解することは必須なのです。
【もっと詳しく知りたい方へ】
【本ウェブサイト内】
・シャペロニンGroEL:私たちが最も深く研究しているシャペロンです。
・新生鎖の生物学:シャペロンは、細胞内でタンパク質ができてくるプロセスである「翻訳」時の新生ポリペプチド鎖(新生鎖)のフォールディングを助けるのが基本です。新生鎖フォールディングにシャペロンがどう関わるかのを調べた研究、さらには(シャペロンが関与する前の)翻訳そのものの研究は近年大きな進展を見せています。
・もっとシャペロンについて知りたい方は、以前のラボHPで掲載していた「シャペロンの基礎 (pdf 1.5MB) 」にたいへん詳しい解説があります。
【外部サイト】・生物物理学会のHPに寄稿したシャペロンの解説もご覧ください。