- A
- A
- A
- 2025.10.10 伊藤隼人が大隅ジャーナル賞を受賞しました(Nucleic Acids Research論文)
- 2025.10.10 伊藤らの成果がNucleic Acids Research誌に掲載されました
- 2025.07.29 幸保明直、池田刀麻が大隅ジャーナル賞を受賞しました
- 2025.07.12 日本RNA学会年会で伊藤隼人がEMBO reports special awardを受賞
- 2025.07.02 Zhuが貢献した共同研究がProtein & Cell誌に掲載されました
- 2025.06.23 日本蛋白質科学会年会で池田刀麻が若手奨励賞優秀賞、新藤英俊がポスター賞を受賞
- 2025.06.15 YouTubeチャンネル始めました
- 2025.04.16 5/17-18 研究室公開のお知らせ(すずかけサイエンスデイ)
- 2025.04.09 大橋らの成果がnpj Biosensing誌に掲載されました
- 2025.04.09 修士課程1名(及川里奈)がラボに加わりました
- 2025.04.01 科研費 基盤研究(S)に採択されました
- 2025.03.29 高校生インターンシップ(研究室体験)を実施しました
- 2025.03.12 蓮見・伊藤らの成果がJ Biol Chem誌に掲載されました
- 2025.03.11 幸保・丹羽らの成果がNature Communications誌に掲載されました
- 2025.03.07 卒研発表で吉田孝太郎が最優秀賞、野口文睦が優秀賞を受賞
- 2025.02.25 池田・野島らの成果がPNAS誌に掲載されました
- 2025.01.29 三輪、田口のIbpAに関する総説がBiological Chemistry 誌に掲載
- 2024.11.21 門倉広らの成果がiScience誌に掲載されました。
- 2024.11.10 学部3年生(黒田旺豊、山田夏碧)がラボに仮配属となりました。
- 2024.09.30 幸保明直、池田刀麻が学振特別研究員に採択(幸保DC2、池田DC1)
- 2024.09.21 高校生インターンシップを開催しました。
- 2024.07.29 PUREシステムに関する総説を J Mol Biol 誌に発表しました。
- 2024.07.02 池田刀麻が第21回国際生物物理会議にて学生ポスター賞を受賞
- 2024.05.27 幸保明直らの成果が J Biol Chem 誌に掲載されました。
- 2024.04.26 茶谷悠平らの成果が Nucleic Acids Research 誌に掲載されました。
- 2024.04.02 修士課程2名がラボに加わりました
- 2024.04.01 坂本素代香が卒研発表で最優秀賞を受賞
- 2024.03.05 坂本素代香、金澤篤宏が令和5年度の高宮賞を受賞
- 2024.01.16 茶谷悠平らの成果が Cell Reports 誌に掲載されました。
- 2024.01.11 伊藤隼人らの成果がScientific Reports誌に掲載されました。
- 2023.12.21 伊藤隼人が第46回日本分子生物学会にてサイエンスピッチ優秀発表賞を受賞。
- 2023.11.10 学部3年生(野口文睦、花市龍世、吉田孝太郎)がラボに仮配属となりました。
- 2023.11.07 伊藤隼人が学術変革(A)領域会議にて学生ポスター賞(最優秀賞)を受賞
- 2023.10.13 伊藤隼人が学振特別研究員DC2に採択
- 2023.08.07 Yajie Chengらの成果が J Biol Chem 誌に掲載されました。
- 2023.08.02 三輪つくみの成果がPNAS誌に掲載されました。
- 2023.07.19 疾患関連の非典型的な翻訳(RAN翻訳)に関する共同研究の論文を発表しました。
- 2023.07.11 池田刀麻が修士論文中間発表会でポスター賞を受賞
- 2023.07.10 池田刀麻が第23回日本蛋白質科学会でポスター賞を受賞
- 2023.07.04 特任准教授と研究支援員がラボに加わりました
- 2023.04.01 修士課程2名と特任講師がラボに加わりました
- 2023.03.31 茶谷悠平特任助教が岡山大准教授として転出
- 2023.03.25 蓮見眞由香が卒研発表で最優秀賞を受賞
- 2023.03.16 シャペロニンGroELの基質タンパク質予測ツールに関する論文を発表しました。
- 2023.02.19 山川絢子が大隅ジャーナル賞を受賞しました(NAR誌論文が対象)
- 2023.02.10 シャペロニンGroELに関する総説を発表しました
- 2023.02.08 山川絢子、丹羽達也、茶谷悠平らの成果がNucleic Acids Research誌に掲載されました
- 2023.02.07 翻訳制御(翻訳アレストやリボソーム不安定化)に関する総説論文を発表しました
- 2023.01.23 伊藤遥介、茶谷悠平らの成果がNature Communicationsに掲載されました
- 2023.01.08 小野寺悠らの成果がMolecular Microbiologyに掲載されました
- 2025.07.14

- 一般向け科学書籍の監修2冊
- これまでに何冊か一般の方々向けの書籍を何冊か執筆した。今年になって小学館より2冊子供向けの書籍を監修したので紹介する。1)ドラえもん科学ワールドspecial 遺伝子のふしぎ 藤子・F・ 不二雄 (イラスト) 2025/7/3 小学館 (→小学館サイト、Amazon)2)10歳からの科学の常識100: 文系の池上彰が教える 池上 彰 (著) 小学館 2025/2/25 (→小学館サイト、Amazon)いずれも、以前池上彰さんと以前の共著、池上彰が聞いてわかった 生命のしくみ 東工大で生命科学を学ぶ 単行本2016年 朝日文庫2020年 朝日新聞出版のご縁で同僚の岩崎博史教授と一緒に監修した。小学生のお子さんがいらっしゃる方はぜひ!

- 2025.10.10

- 伊藤らの成果がNucleic Acids Research誌に掲載されました
- Canonical translation factors eIF1A and eIF5B modulate the initiation step of repeat-associated non-AUG translation. Hayato Ito, Kodai Machida, Yuzo Fujino, Mayuka Hasumi, Soyoka Sakamoto, Yoshitaka Nagai, Hiroaki Imataka, Hideki Taguchi Nucleic Acids Res 2025 Sep 23;53(18):gkaf994. https://doi.org/10.1093/nar/gkaf994 (open access) 近年、筋萎縮性側索硬化症(ALS)など神経変性疾患患者が保持する遺伝的変異に起因する非典型的な翻訳が知られるようになってきました。例えば、ALSではGGGGCCという塩基リピートが異常に伸長し、そのリピートを含む領域から開始コドンAUGがなくても翻訳が開始して毒性をもつペプチドができるという現象で、リピート関連非AUG(Repeat-Associated Non-AUG: RAN)翻訳と呼ばれています。本研究では兵庫県立大学の今高さん、町田さんらが開発したヒト因子由来の翻訳再構成系(ヒトPURE)を駆使して、RAN翻訳に重要な翻訳因子(eIF1A、eIF5Bなど)を同定し、その機能解明を行いました。

- 2025.06.21

- NHK「人体III」のサプリメント(補足):謝辞
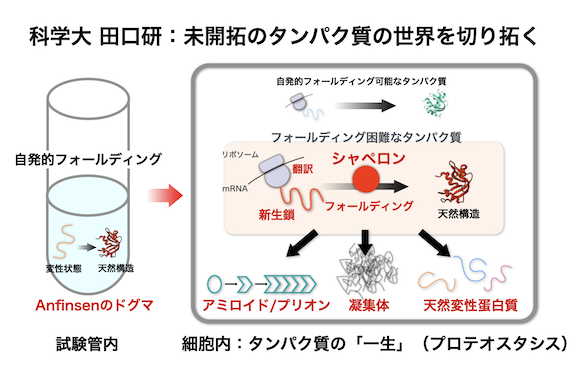
- NHKスペシャル「人体III」の最終回(6/15放映)で私のライフワークのシャペロニンを取り上げていただいた。「人体III」シリーズ4回の全体を貫くテーマは「細胞」、特に細胞内ではたらくタンパク質(細胞内キャラクター)に焦点を当てている。最終回の序盤で、細胞内キャラを育てるキャラクターということでシャペロンが登場する。観ておられない方のために概要をお伝えしよう。1.オルセー美術館に収蔵されているルノアールの「ムーラン・ド・ラ・ギャレット」が映される。Pierre-Auguste Renoir, "Le Moulin de la Galette" from Wikimedia Commons2.この絵画を使ってJudith Frydman博士(スタンフォード大)がシャペロンの概念を解説する。Frydman博士は真核生物シャペロニンの圧倒的なリーダーである3.細胞内で赤ちゃんタンパク質(新生鎖)がリボソームから産まれてくるようすが「人体」シリーズお得意のCGで解説される。ぶらぶらしたヒモ状態の新生鎖が働けるかたちに折りたたんでいくようすが紹介される(注1)。4.新生鎖は絡まって凝集体になりうるリスクがあるので、それを防ぐためにシャペロニンが空洞内に新生鎖を閉じ込めて成長させる。5.最後に私が10秒ほど登場して、「シャペロンはバクテリアからヒトまでどんな細胞にもどっさりと含まれていて、いろんな細胞内キャラが自らの能力を発揮できるようにするためになくてはならないキャラクターだ」と言って締める。「シャペロンは細胞内にどっさり含まれている」というところで、ヒト細胞でシャペロン(Hsp70-GFP)が発現しているようすの蛍光顕微鏡動画が映る。という流れである。番組のエンドロールの協力者は該当部分で一人だけということで私の名前しか出なかったが、本来NHKの方にお願いしていたのは以下の方々である。この場を借りて御礼申し上げます。伊藤隼人さん:現在私のラボの博士課程学生で疾患関連塩基リピートによる非AUG(RAN)翻訳を研究している。最近ライブイメージングも行っているので、番組ディレクターから要請のあったシャペロンが細胞内にどっさりあるようすをHsp70ーGFPを内在プロモーターで発現させて動画を作ってもらった。実際には、細胞に熱ストレスをかけてシャペロンが大量に発現するところなども見せたいということだったが見送りになった。ヒトの培養細胞(U2OS細胞)でのHsp70-sfGFP発現のようす川上勝さん:私のインタビュー画面で私が持っているシャペロニン模型は川上勝さん(現在神戸大)が考案した作成法で作られた特別な模型である(Kawakami-model)。川上さんは私がGroEL研究者ということでずっと貸し出してくれており、本ブログでもたびたび紹介している(→「シャペロニンの模型が手元に!」2013.7.27)。このような印象的なタンパク質模型に興味ある方はスタジオミダスさんのウェブサイトをご覧下さい。Kawakami ModelによるGroELーGroES複合体模型上村英里さん:この番組の当初の構想では、私があちこちで好んで使っている「シャペロンがあるとゆで卵にならない」実験を実際にやってみましょう、という話しが進んでいた。久々の実験だったので古い好熱菌のシャペロニンをフリーザーから発掘して私自身で予備実験するとともに、それだけでは足りなかったので、技術補佐員の上村英里さんにシャペロニンの精製などを行ってもらった。結局見送りになった・・・。注1:ここで「ひもには磁石のようにくっつきやすい部分があり、自然と「働ける形」になろうとする」という説明があった。専門用語的にはCotranslational folding(リボソームでの翻訳に共役した折りたたみ)で、基本的にはタンパク質は自発的に折りたたむという原理、すなわちAnfinsenのドグマが表現されている。ただし、「磁石」の例えは不適切でないか、それより、プラスとマイナスが近づく(つまり静電相互作用)などの例えがよいのでは、と指摘していたが、わかりやすさが優先されたようだ。「ムーラン・ド・ラ・ギ

- 2025.07.29

- 幸保明直、池田刀麻が大隅ジャーナル賞を受賞しました
- 幸保明直(Nature Communications誌)、池田刀麻(Proc Natl Acad Sci USA誌)の二人が筆頭著者の掲載論文が大隅ジャーナル賞を受賞しました(→生命理工学系サイト)。 [caption id="" align="aligncenter" width="430"] 幸保明直(右)と粂生命理工学院長[/caption] [caption id="" align="aligncenter" width="430"] 池田刀麻(右)と粂生命理工学院長[/caption] 注)大隅ジャーナル賞とは、以下のような趣旨で設立された学内の学生向けの賞です(→生命理工サイト)。 東京工業大学は、2016年ノーベル生理学・医学賞を受賞した大隅良典栄誉教授からの多額の寄附を原資として「大隅良典記念基金」を設置しました。本基金は、将来の日本を支える優秀な人材の育成、および長期的な視点が必要な基礎研究分野における若手研究者等の育成の推進など、研究分野の裾野の拡大を目的としています。大隅ジャーナル賞は、大隅良典記念基金を原資として、優秀な論文が掲載された生命理工学院の学生を表彰し、学資一時金を支給するもので、2017年4月に顕彰を開始しました。